احیا فرومنگنز با گاز حاوی متان با دمای پایین را میتوان با استفاده از گاز حاوی متان با فعالیت کربن بالا یا با احیای کربوترمال تحت فشار جزئی CO انجام داد.استفاده از گاز طبیعی به جای کربن جامد برای تولید فرومنگنز روشی رو به جلو در توسعه پایدار است. فرآیندهای پیرومتالورژی صنعتی در متالورژی آهنی بر اساس احیای کربوترمال اکسیدهای فلز است. احیا کربنی اکسیدهای پایدار به دماهای بالا نیاز دارد. ا در شرایط استاندارد، متان از نظر ترمودینامیکی بالای 550 درجه سانتی گراد ناپایدار است و ترک می خورد و به کربن جامد و هیدروژن تجزیه می شود. در نسبت و دمای مناسب CH4/H2، فعالیت کربن در فاز گازی حاوی متان میتواند نسبت به گرافیت بسیار بالاتر از حد باشد، که شرایط ترمودینامیکی مطلوبی را برای احیا فراهم می کند. برای حفظ این شرایط، نسبت سرعت احیا/کربندهی باید بیشتر از میزان رسوب کربن جامد باشد. در این مقاله احیا اکسیدهای منگنز خالص در دماهای نسبتا پایین مورد بحث قرار گرفت. این فرآیند شامل تزریق گاز طبیعی حاوی متان به فرومنگنز مذاب است. گازهای هیدروژن و CO اکسیدهای جامد منگنز و اکسیدهای آهن در سنگ معدن منگنز را به منگنز و آهن در راکتور فرومنگنز احیا (در واقع احیا فرومنگنز با گاز حاوی متان صورت می گیرد) می کنند. بخشی از گاز بسیار احیا کننده به دست آمده برای احیا سنگ آهن در یک راکتور احیا مستقیم برای تولید DRI قابل استفاده است و بقیه در یک واحد بازیافت انرژی برای تولید برق مورد استفاده قرار می گیرد. یک گاز داغ با مقدار قابل توجهی CO و H2 از راکتور خارج می شود و از طریق استفاده از متان در یک اصلاح کننده گاز به یک مخلوط گاز غنی CO-H2 ارتقا می یابد. راکتور فرومنگنز ارائه شده نشان از پایداری بیشتر فرآیند به نسبت فرآیند تولید تجاری فرومنگنز فعلی است و کاربرد آن با حدود 45 درصد مصرف انرژی الکتریکی کمتر همراه است.
1. مقدمه
تولید تجاری فرومنگنز از طریق ذوب کربوترمی – احیا فرومنگنز با گاز حاوی متان با استفاده از فناوریهای کوره قوس غوطهور (SAF) و کوره بلند (BF) است. فن آوری SAF امروزه با توجه به چندین مزیت آن در مقایسه با BF، غالب است. کک متالورژیکی اصلی ترین احیا کننده کربن جامد است که در SAF استفاده می شود. وابستگی فرآیند به استفاده از کربن جامد در اصل مربوط به ترموشیمی احیا مونوکسید منگنز (MnO) است که توسط کربن قابل احیا است و نه توسط گازهای H2 و CO اصولاً احیا فرومنگنز با گاز حاوی متان با اکسیدهای غنی از منگنز (MnO2، Mn2O3 و Mn3O4) به MnO توسط گازهای H2 و CO امکان پذیر است. گاز طبیعی که سرشار از متان (CH4) است، جایگزین پایدارتری برای تولید فلز و فرومنگنز در مقایسه با کک متالورژیکی است و بنابراین، علاقه تحقیقاتی قابل توجهی در استفاده از این احیا کننده وجود داشته است. با این حال، استفاده از گاز طبیعی در دماهای بالا باعث تولید مخلوطهای گاز CO و H2 میشود و احیا توسط این گازها نمیتواند فراتر از MnO ادامه یابد و این مبنای بسیاری از محققان برای استفاده از گاز طبیعی برای پیش احیا سنگ معدنی است که قبلاً بررسی شد. متان از نظر ترمودینامیکی بالای 550 درجه سانتی گراد ناپایدار است و به جامد تجزیه می شود. فعالیت کربن در فاز گاز حاوی متان میتواند نسبت به گرافیت بسیار بالاتر و موثرتر باشد، که شرایط ترمودینامیکی مطلوبی را برای احیا فراهم می کند. برای حفظ این شرایط، نرخ احیا فرومنگنز با گاز حاوی متان/کربن دهی باید بیشتر از میزان رسوب کربن جامد باشد.
2. تئوری و پیشینه تحقیق
MnO را می توان از طریق یک احیاء کربوترمی از طریق واکنش شیمیایی 1 به منگنز فلزی احیا کرد و گاز CO تولید شده را برای احیا اکسیدهای غنی از منگنز به منگنز از طریق واکنش های شیمیایی 2 الی 7 استفاده کرد اما استفاده از یک واحد پیش احیا مبتنی بر گاز طبیعی (احیا فرومنگنز با گاز حاوی متان) برای پالایش سنگ معدن منگنز از نقطه نظر عرضه عامل احیا سودمند نیست. بدیهی است که استفاده از متان در یک واحد پیش احیاء جداگانه (مستقیم یا غیرمستقیم پس از اصلاح آن به H2 + CO) و سپس احیا MnO توسط کربن جامد در مرحله ذوب، مصرف کلی کربن در واحد جرم منگنز تولیدی را افزایش خواهد داد. به بیان دقیق، وضعیت ایده آل حداکثر استفاده از CO است که از طریق واکنش 1 برای واکنش های 2-4 بدون استفاده بیشتر از کربن (C از منبع متان) تولید می شود. علاوه بر این، واکنشهای احیا اکسیدهای منگنز توسط مخلوطهای گازی H2 و CO (احیا فرومنگنز با گاز حاوی متان -منشأ گرفته از متان) که در آن واکنشهای کمتر گرمازای 5-7 نسبت به واکنشهای 2-4 به طور همزمان انجام میشوند، نسبت به مسیر کربوترمیک برای بهره بردن از انرژی فرآیند سودمند نیستند.
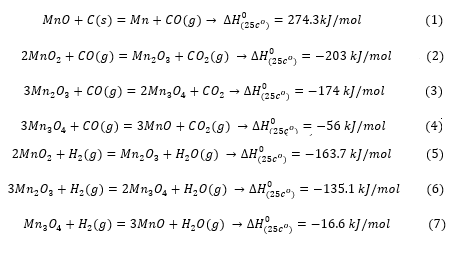
در تولید فرومنگنز در SAF، کربن جامد موجود در شارژ در تماس با گازهای CO/CO2 است و بنابراین، واکنش بودوار (8) رخ می دهد و باعث از دست دادن مواد کربنی و اتلاف انرژی الکتریکی شده و انتشار CO2 بیشتر در واحد جرم محصول فروآلیاژ نسبت به حالت ایده آل فرآیند بدون واکنش بودوار رخ می دهد.
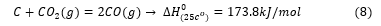
از آنجایی که در این واکنش 2 مول CO به ازای هر 1 مول CO2 مصرفی تولید می شود و در نهایت از طریق احتراق گاز خروجی SAF توسط هوا به CO2 اکسید می شود، دو برابر بیشتر از CO2 مصرف شده توسط واکنش بودوار تولید می شود. واکنش بودوار در SAF باعث استفاده بیشتر کربن میشود و به ازای هر تن آلیاژ تولید شده، چند صد کیلووات ساعت انرژی الکتریکی مصرف میکند، یعنی 400 کیلووات ساعت برای 475 کیلوگرم مصرف کک مصرفی به ازای هر تن فروآلیاژ تولید شده. بنابراین، توسعه فناوری برای انجام پیش احیا سنگ معدن به MnO به طور جداگانه و سپس احیا کربوترمیک در کوره ذوب سودمند است و ادعا شده است که در صورت استفاده از مواد خام پیش گرم شده در دماهای 550، 650 و 950 درجه سانتی گراد، مصرف انرژی الکتریکی مورد نیاز برای احیا (احیا فرومنگنز با گاز حاوی متان) به ترتیب 8.8، 13.5 و 20.4 درصد کاهش می یابد. در مدل پیشنهادی گاز طبیعی (متان) پیشگرم شده که عمدتاً از اجزای H2، CO، CO2 و H2O با ارزش شیمیایی بالا (H2 و CO) تشکیل شده است، به طور مستقیم در راکتور FeMn تزریق می گردد.
3. روش تحقیق در اتباط با احیا فرومنگنز با گاز حاوی متان
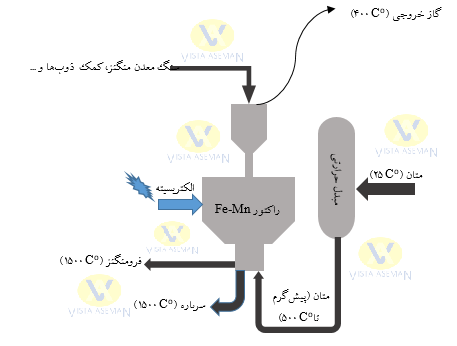
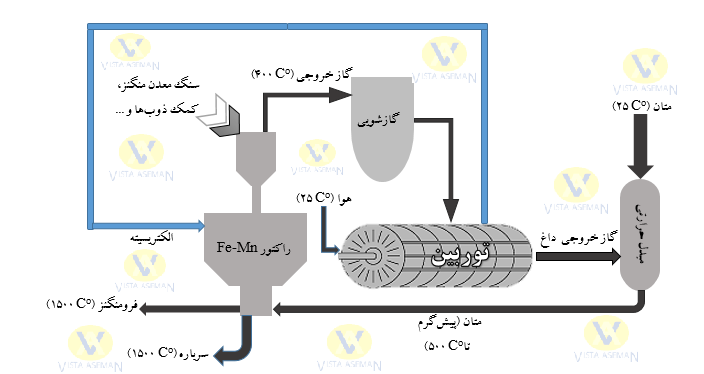
مطالعه ترموشیمی فرآیند ترک خوردگی متان FeMn/CH4 و محاسبات مربوط به موازنه مواد و انرژی به شرح زیر انجام شد. برای انجام تعادل جرم و انرژی مناسب، از داده های بنیادی در مورد احیا سنگ معدن منگنز و آهن استفاده شد. محاسبات تعادل در صورت نیاز انجام شد. رویههای کاربردی محاسبات به طور مفصل شرح داده شدهاند تا خوانندگان رشتههای مهندسی مختلف با پیشینههای مختلف بتوانند کار را دنبال کنند و شیمی حرارتی فرآیند را درک کنند. برای انجام محاسبات اصلی احیا فرومنگنز با گاز حاوی متان از ماژول تعادل حرارت و مواد در نرم افزار HSC Chemistry نسخه 9 استفاده شد. برای هر مرحله فرآیند، داده های ورودی برای محاسبات، مقدار و دمای اجزای موجود در خوراک و مقدار محصولات و دمای آنها در خروجی در نظر گرفته شد و نرم افزار تعادل جرم و انرژی را برای فرآیند یا مراحل تعریف شده فرآیند انجام داد. شکل 1 شماتیکی کلی از فرآیند را نمایش می دهد.
4. نتایج و بحث
4-1. تشریح مدل احیا فرومنگنز با گاز حاوی متان
احیا کربوترمی متان در دماهای بالا و عمدتاً از سرباره اشباع شده از MnO در ناحیه بستر کک رخ می دهد. روابط فازی برای فرآیند احیا MnO از سرباره در ادبیات قبلی گزارش شده است و به طور تجربی نشان داده شده است که احیا کربوترمیک MnO توسط کربن جامد (ذرات کک) و کربن محلول در فرومنگنز با کربن بالا اتفاق میافتد. سینتیک احیا MnO توسط کربن محلول در آلیاژهای Fe و Fe-Mn سریع است و منگنز با سرعت بالایی از سرباره به فاز فلزی منتقل میشود. مطالعات در مورد احیا MnO از سرباره ها توسط کربن جامد، انرژی فعال سازی را در محدودهkJ/mol 332-447 نشان می دهد، در حالی که احیا کربن محلول در مذاب Fe-Mn از طریق انرژی فعال سازی به طور قابل توجهی کمتر بوده در محدوده kJ/mol 90-197 رخ می دهد. بنابراین، احیا MnO از سرباره فرومنگنز تنها توسط کربن محلول در فلز بدون استفاده از مواد حاوی کربن جامد انجام می شود، اگر تماس سرباره/فلز برای دستیابی به سرعت مناسب به موقع اتفاق بی افتد. بطورکلی احیا کربنی اکسیدهای فلزی پایدار مانند MnO به دماهای بالا نیاز دارد. احیا فرومنگنز با گاز حاوی متان در دمای پایین را می توان با استفاده از گاز حاوی متان با کربن بالا، یا با احیا کربوترمال تحت فشار جزئی CO انجام داد. مزایای احیا گازی نسبت به احیا کربوترمال عبارتند از: الف) دمای عملیاتی کمتر، ب) توانایی تصفیه ریز ذرات، ج) سینتیک سریع تر و د) حذف کک. در شرایط استاندارد، متان از نظر ترمودینامیکی در دماهای بالاتر از 550 درجه ناپایدار است و مطابق با واکنش (9) ترک میخورد (تجزیه به کربن جامد و هیدروژن میشود).
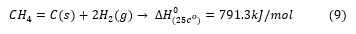
اگر نسبت CH4/H2 بهینه و دمای فرآیند نیز مناسب باشد، فعالیت کربن در فاز گاز حاوی متان میتواند شرایط ترمودینامیکی مطلوبی را برای احیا در دماهای نسبتاً پایین نسبت به گرافیت فراهم کند. پتانسیل و محدودیت در احیا اکسیدهای فلزی توسط گاز حاوی متان را می توان با توجه به احیا سنگ آهن نشان داد. احیا هماتیت توسط گاز حاوی متان را می توان با واکنش کلی زیر ارائه کرد:
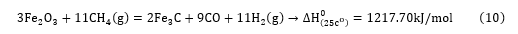
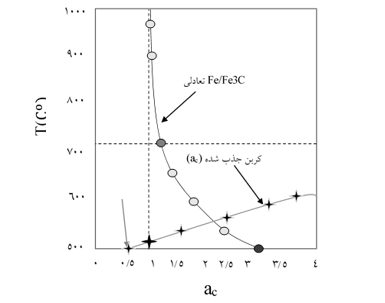
Fe3C فاز ناپایداری است و به سرعت به آهن و کربن تجزیه می شود. عملکرد این کربن تجزیه شده بر اساس دمای فرآیند طبق دیاگرام آهن کربن در شکل 2 نشان داده شده است. ناپایداری ترمودینامیکی سمنتیت با کاهش دما افزایش می یابد. شکل 2 همچنین فعالیت کربن در مخلوط گاز CH4-H2-Ar (35 درصد حجمی CH4 و 55 درصد حجمی H2) را نشان می دهد. از شکل 2 می توان نتیجه گرفت که تشکیل سمنتیت با احیا اکسیدهای آهن با استفاده از مخلوط گاز CH4-H2-Ar در دمای بالاتر از 571 درجه سانتیگراد رخ می دهد.
فرآیند احیا با جذب متان در محلهای فعال سطح اکسید و تجزیه آن به کربن و هیدروژن آغاز میشود. واکنش کلی جذب متان و ترک خوردگی را می توان به صورت واکنش 17 ارائه کرد:

که در آن Cadنشان دهنده گونه های کربن فعال جذب شده بر روی سطح جامد است که به طور قابل توجهی با کربن جامد رسوبی متفاوت است. این کربن جذب شده فعال، احیا پذیری و سرعت احیا بیشتری را در مقایسه با احیا کربوترمال فراهم می کند. بر اساس این واکنش (17)، فعالیت ترمودینامیکی کربن جذب شده را می توان با گرافیت به عنوان حالت استاندارد تعریف کرد:
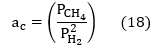
کربن جذب شده توسط واکنشهای احیا/ سمنتاسیون مصرف میشود. عامل کلیدی نرخ بالای واکنش احیا در مقایسه با نرخ رسوب کربن است. اگر کربن جامد روی سطح نمونه تشکیل شود، دسترسی گاز احیاکننده به اکسیدهای فلزی را مسدود میکند و فعالیت کربن در سطح اکسید بدون در نظر گرفتن نسبت بالای PCH4/(PH2)2 در گاز ورودی کاهش می یابد. بنابراین، شرایط سخت زیر برای احیای اکسیدهای فلزی توسط گاز حاوی متان را می توان فرموله کرد.
سرعت احیا/سمنتاسیون باید بیشتر از میزان رسوب کربن جامد باشد. احیا و نرخ رسوب کربن متاثر از دما و ترکیب گاز (نسبت متان به هیدروژن) و سطح اکسید است که به اندازه ذرات، تخلخل و اندازه منافذ بستگی دارد. واکنش رسوب کربن جامد به شدت تحت تأثیر کاتالیزورها قرار می گیرد.
4-2. احیا اکسیدها و سنگ معدن منگنز توسط گاز حاوی متان
اکسید منگنز (MnO) توسط متان به کاربید منگنز با واکنش زیر احیا می یابد و در شکل 3 دیاگرام تعادلی کربن- منگنز برای درک بهتر نمایش داده شده است:
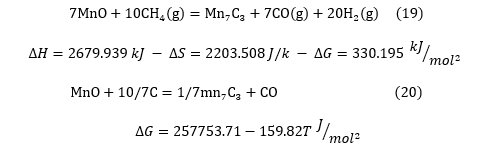
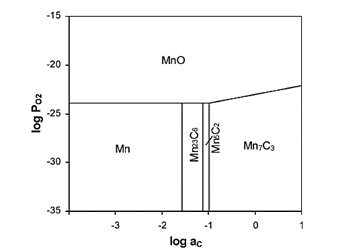
در شرایط استاندارد، واکنش (19) به طور خود به خود در دمای بالاتر از 928 درجه سانتی گراد ادامه مییابد، در حالی که احیا کربوترمال MnO از 1340 درجه سانتیگراد(شرایط استاندارد) شروع میشود. بر همین اساس نمودار تغییرات آنتالپی این واکنش بر حسب دما در شکل 4 نمایش داده شده است.
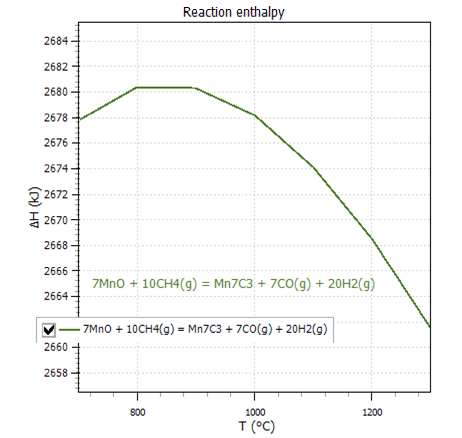
Oleg Osterovsky و همکارانش نتایج فرآیند دمایی احیا از MnO2 توسط مخلوط گاز را به صورت نمودار تعادلی درآوردند که در شکل 4 نشان داده شده است.
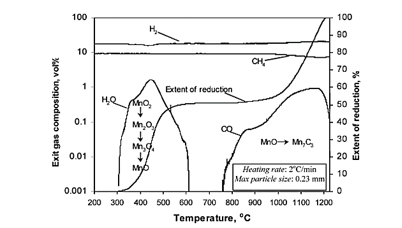
بر اساس شکل 4، احیا با تبدیل MnO2 به Mn2O3، Mn3O4 و MnO توسط هیدروژن صورت گرفت (فقط H2O در فرآیند تولید شد). این واکنش در 610-620 درجه سانتی گراد کامل می شود. تشکیل کاربید منگنز با احیا MnO از 760 درجه سانتی گراد آغاز شده و در حدود 1200 درجه سانتی گراد تکمیل می شود. در ادامه برای ارزیابی پایداری فرآیند احیا فرومنگنز با گاز حاوی متان ارائه شده، مصرف انرژی الکتریکی و انتشار CO2 از فرآیند با اعداد صنعتی موجود برای فرآیند SAF مقایسه میشوند. بر اساس محاسبات موجود در مطالعه ی Safarian ، در صورتی که متان مورد استفاده تا 500 درجه سانتی گراد پیش گرم شده باشد، حدود 1824 کیلووات ساعت انرژی الکتریکی در هر تن فرومنگنز تولیدی برای راکتور مستقل HC-FeMn مورد نیاز است. این بدیهی است که این ارزش نظری برای موردی است که گاز فرآیند FeMn بازیابی نشده و یا در فرآیندهای دیگر مورد استفاده قرار نگیرد. براساس مستندات این مطالعه در مورد یک راکتور HCFeMn مستقل با واحد بازیابی انرژی حدود 1063 کیلووات ساعت بر تن FeMn، با در نظر گرفتن بازده 45 درصدی توسط توربین بازیافت می شود. بنابراین، انرژی الکتریکی خالص مورد نیاز حدود 867.2 کیلووات ساعت بر تن FeMn است که به طور قابل توجهی کمتر از یک راکتور FeMn بدون بازیابی انرژی است. بدیهی است که مصرف انرژی الکتریکی با استفاده از توربینهای کمبازده افزایش مییابد و مصرف انرژی فرآیند کمی بیشتر از راکتور مستقل FeMn است. اما اگر این فرآیند توسعه داده شود و از گاز خروجی آن در فرآیند تولید DRI استفاده شود (روش Douplex) ارزش افزوده بیشتری ایجاد شده و شرایط مطلوب تری را رقم می زند. راکتور مستقل FeMn با واحد بازیابی انرژی (شکل 6) می تواند جایگزینی برای SAF برای صنعت فروآلیاژ باشد.
5.نتیجه گیری
در احیای اکسیدهای فلزی توسط گاز حاوی متان، فعالیت کربنی بالای گاز احیا کننده کلید دستیابی به سرعت و میزان بالای احیا اکسیدهای فلزی توسط گاز حاوی متان است. همچنین باعث رسوب کربن جامد می شود که یک اثر کندکنندگی قوی در فرآیندهای احیا دارد. نرخ احیا/سمنتاسیون باید بیشتر از میزان رسوب کربن جامد باشد. این شرایط در احیای اکسیدهای خالص منگنز، صدق میکند. با این حال، در احیای سنگ معدن، نرخ تشکیل کربن جامد بیشتر از نرخ احیا است، که یک محدودیت ذاتی در اجرای صنعتی فرآیندهای احیا با استفاده از گاز طبیعی است. رویکرد جایگزین می تواند مبتنی بر استفاده از گاز طبیعی به عنوان منبع کربن و هیدروژن برای احیای کربوترمال اکسیدهای فلز در هیدروژن باشد. با در نظر گرفتن ترموشیمی فرآیند نتایج اصلی این کار به شرح زیر است:
- فرآیند تولید فرومنگنز توسط گاز طبیعی از دیدگاه شیمی، در راکتور FeMn قابل دوام است و محصولی گازی با مقادیر بالایی از گازهای CO و H2 تولید میکند.
- خروجی گاز رآکتور FeMn را می توان به یک گاز احیاکننده داغ برای تولید DRI از طریق ریفورم متان در یک اصلاح کننده گاز ارتقا داد.
- بازیافت انرژی از گازها در این فرآیند به طور قابل توجهی با حدود 45 درصد در واحد جرم فلزات تولید شده، به این فرآیند کمک می کند.
احیا دمای پایین را می توان با استفاده از گاز حاوی متان با فعالیت کربن بالا یا با احیای کربوترمال تحت فشار جزئی CO انجام داد.
در شرایط استاندارد، متان از نظر ترمودینامیکی بالای 550 درجه سانتی گراد ناپایدار است و ترک می خورد و به کربن جامد و هیدروژن تجزیه می شود. در نسبت و دمای مناسب CH4/H2، فعالیت کربن در فاز گازی حاوی متان میتواند نسبت به گرافیت بسیار بالاتر از حد باشد، که شرایط ترمودینامیکی مطلوبی را برای احیا فراهم می کند.
تولید تجاری فرومنگنز از طریق ذوب کربوترمی – احیا سنگ معدن منگنز با استفاده از فناوریهای کوره قوس غوطهور (SAF) و کوره بلند (BF) است. فن آوری SAF امروزه با توجه به چندین مزیت آن در مقایسه با BF، غالب است. کک متالورژیکی اصلی ترین احیا کننده کربن جامد است که در SAF استفاده می شود. وابستگی فرآیند به استفاده از کربن جامد در اصل مربوط به ترموشیمی احیا مونوکسید منگنز (MnO) است که توسط کربن قابل احیا است و نه توسط گازهای H2 و CO اصولاً احیا اکسیدهای غنی از منگنز (MnO2، Mn2O3 و Mn3O4) به MnO توسط گازهای H2 و CO امکان پذیر است.
نویسندگان: متین پاشاخانلو، امیرحسین یوسف بیگی، عباس پارسا.
جهت کسب اطلاعات تکمیلی با ما در تماس باشید.