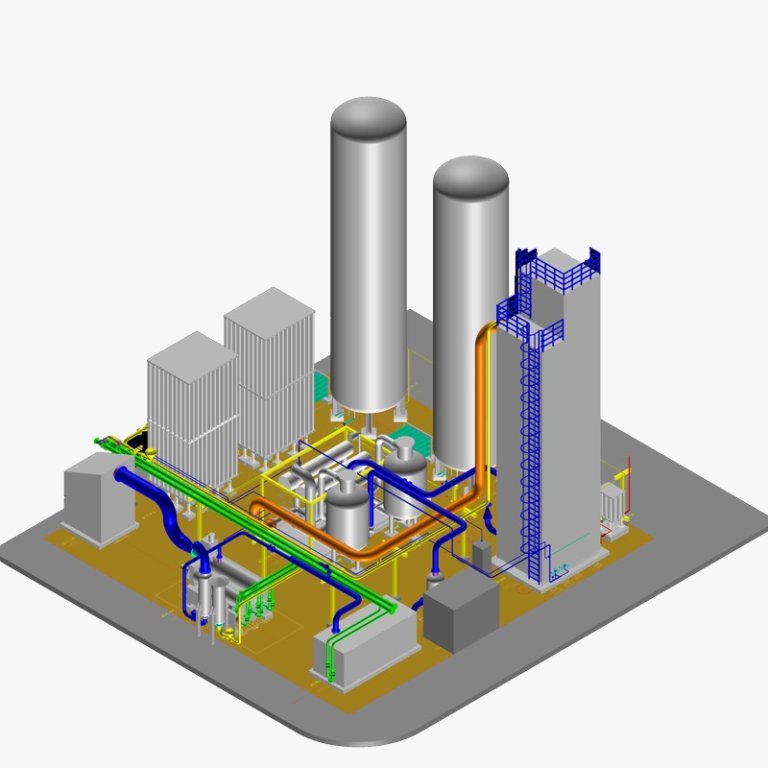
روش های تولید گازهای صنعتی و طبی:
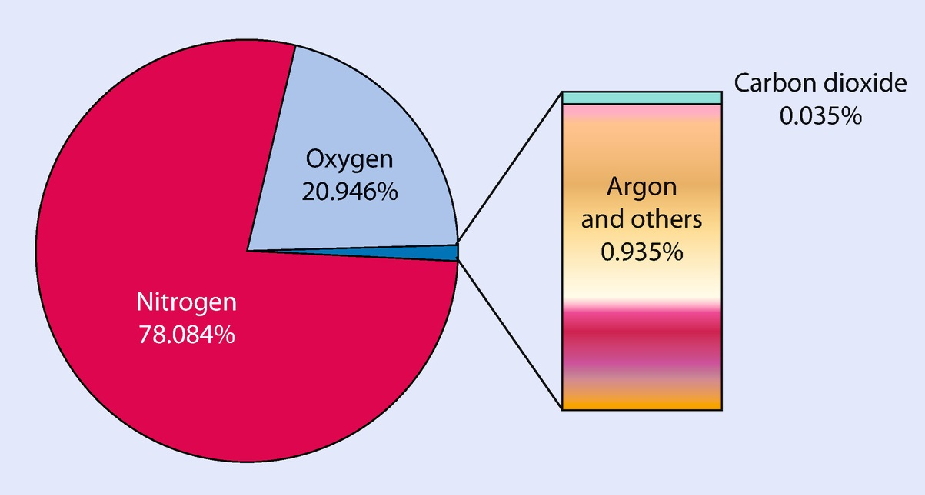
هوایی که ما تنفس میکنیم متشکل از 21 % اکسیژن، 78 % نیتروژن و یک درصد مابقی گازهایی از جمله دی اکسید کربن، گازهای بی اثر، اکسیدهای نیتروژن، گوگرد و … است. وجود هوا برای زیست جانداران هوازی (از حیوانات تا گیاهان و میکروبها) ضروری است. هوای محیط بسته به ارتفاع از سطح دریا و عوامل انسانی مانند سطح آلودگی متفاوت است. هرچه هوا به سطح دریا نزدیکتر باشد، درصد اکسیژن بیشتر است.
نام اکسیژن از کلمه یونانی oxy (به معنای اسیدی – تیز) و لاتین gen (به معنی تولید) تشکیل شده است که معنای تحت الفظی غلط تولید اسید را می دهد. این اعتقاد اشتباه برای اولین بار توسط لاوازیه مطرح شده بود. این گاز که از سال 1790 به بعد اکسیژن نامیده شد، برای نخستین بار در سال 1774 (با نام Dephlogisticated) کشف شد. تولید این گاز در دهه های اخیر در مقیاس بزرگ در دماهای پایین به صورت تقطیر هوای مایع یا دوره های معمولی با استفاده از مواد جاذب انجام می شود. این مواد جاذب عمدتاً غربالهای مولکولی هستند. در این روش با حذف نیتروژن از هوا اکسیژن و آرگون تولید می شود. این گاز در دهه 80 میلادی تقریباً چهارمین رتبه از نظر حجم تولید در جهان را داشته است.
نام نیتروژن نیز از کلمات لاتین (Niter یاNitrum ) به معنای شوره و (gen) تشکیل شده است و از سال 1790 به بعد به کار برده شد. این اسم تداعی موادی را می کند که دارای ترکیب شوره هستند، مانند جوهر شوره که نام مستعار آن اسید نیتریک (HN03) می باشد. این گاز تقریبا پنجمین رتبه را از نظر حجم تولید در دهه 80 میلادی دارا بوده است که فرآوری آن در مقیاس صنعتی به وسیله تقطیر جزئی هوای مایع مسیر می باشد. این گاز از تجزیه آمونیاک نیز به دست می آید.
آرگون نیز همانطور که از اسمش پیداست به معنای غیر فعال می باشد که از کلمه یونانی (Argos) گرفته شده است که به وضوح خاصیت و طبیعت خنثی این گاز را در شرایط عادی نشان می دهد. این نام برای اولین بار در سال 1894 به کار برده شد.
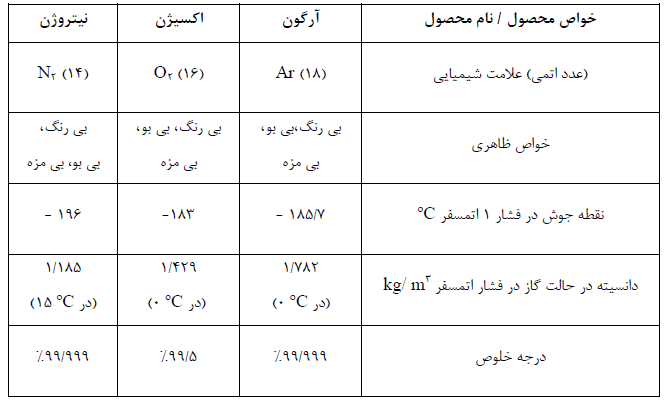
به طور کلی مشخصات فنی براساس خواص ظاهری مانند: رنگ، بو، طعم، برخی خواص شیمی فیزیکی، علامت یا فرمول شیمیایی، عدد اتمی و در نهایت درجه خلوص اکسیژن، آرگون و نیتروژن مطابق جدول ذیل می باشد:
موارد کاربرد گازهای اکسیژن، نیتروژن و آرگون:
آرگون: ساخت قطعات الکترونیکی، جوشکاری های حساس و نیز به عنوان ماده اولیه لامپ سازی و غیره می باشد.
اکسیژن: صنایع جوشکاری، برشکاری، فولاد سازی، ریخته گری، شیمیایی و همچنین پزشکی می باشد. اکسیژن عمدتاً به عنوان کالای واسطه ای در صنایع سرماسازی، نگه داری مواد غذایی (به صورت نیتروژن مایع) و صنایع الکترونیک، عملیات حرارتی و … کاربرد دارد.
نیتروژن: صنایع سرماسازی، نگهداری مواد غذایی (به صورت نیتروژن مایع) صنایع الکترونیک، عملیات حرارتی و شستشوی خطوط لوله و بعضی دستگاههای شیمیایی و به طور کلی در صنایع شیمیایی به عنوان ماده اولیه بعضی محصولات با استفاده های جانبی کاربرد دارد.
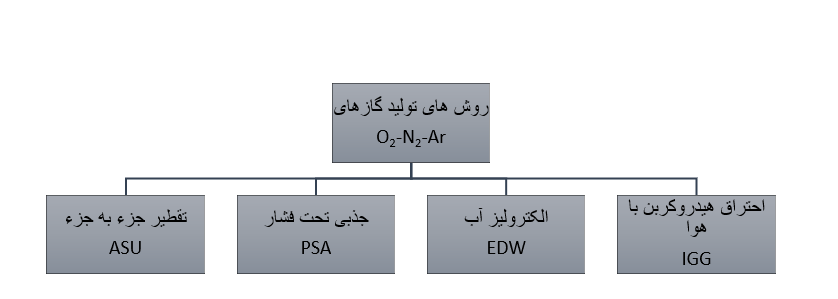
روشهای تولید گازهای اکسیژن، نیتروژن و آرگون:
1- احتراق هیدروکربن با هوا (IGG: Inert Gas Generator)
گاز طبیعی با پروپان و هوا سوزانده می شود. بعد از جداسازی محصولات حاصل از احتراق، نیتروژن خالص باقی می ماند. قبل از ورود به مشعل، نسبت هوا و گاز طبیعی مورد نیاز تنظیم می شود. در محفظه احتراق، گاز طی یک فرآیند گرمازا و به طور کامل سوزانده می شود. گازهای حاصل از احتراق حاوی H2O, Co2, N2 و مقادیر کمی H2, Co می باشد. گازها در یک کندانسور صفحه ای خنک می شوند و از یک جدا کننده بخار، آب کندانس شده، جدا می شود. پس از آن گازهای حاصل از یک خشک کن تبریدی که طی آن نقطه شبنم تا حدود 4 درجه سانتی گراد تقلیل می یابد، عبور داده می شود. دی اکسید کربن و بخار آب مازاد در بستر غربال ملکولی (که به طور متناوب از دو بستر استفاده می شود) جذب و حذف می شوند. در یک بستر گازها تخلیص و در بستر دیگر عمل فعال سازی صورت می گیرد (توسط پمپ خلاء)، محصول نیتروژن حاوی ppm500 دی اکسید کربن و ppm1000 مونواکسید کربن با نقطه شبنم 60 درجه سانتیگراد، با فشار اندکی بالاتر از فشار اتمسفر یک می باشد.
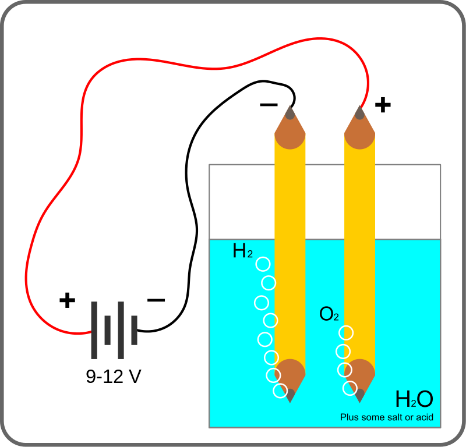
2- تولید اکسیژن به روش الکترولیز آب (EDW: Electrolytic Dissociation of Water)
فرایندی متداول جهت تجزیه آب به عناصر سازنده آن یعنی اکسیژن و هیدروژن است که در آن از یک جریان الکتریکی مستقیم و دو الکترود بهره گرفته میشود. از منبع جریان برق DC برای دو الکترود یا صفحه فلزی (از فلزات نجیب نظیر پلاتین یا ایریدیم) استفاده میشود که هر دو الکترود وارد آب میشوند و از آنجا که آب خالص رسانایی ناچیز و هدایت جریان الکتریکی یک میلیونیم آب دریا دارد باید مقداری الکترولیت (اسید، باز یا نمک فلزی) اضافه شود. در مجاورت الکترود آند آب اکسایش میابد و سبب تولید اکسیژن، پروتون و الکترون میشود که گازهای اکسیژن تولید شده بصورت حباب از ظرف نیم واکنش آندی خارج میشود و الکترونهای تولید از طریق الکترود آندی به بخش الکترود کاتدی حرکت میکند و یونهای هیدروژن ایجاد شده از طریق غشای مبادله کننده پروتون به بخش الکترود کاتدی میروند و با الکترونهای موجود سبب کاهش هیدروژن و تولید حبابهای هیدروژن میشود.
در این فرایند آب به عناصر سازنده اش یعنی اکسیژن و هیدروژن H2O تجزیه میشود. مولکول آب که از دو عنصر فوق بصورت دو یون مثبت هیدروژن و یک یون منفی اکسیژن شکل گرفته است. توسط جذب الکترو مغناطیسی از هم جدا میشوند . وقتی الکتریسته از طریق دو الکترود به آب وارد میشود یک کاتد (منفی) و یک آند(مثبت)، این یون ها به الکترود با بار غیر همنام جذب میشوند. یعنی یون های هیدروژن با بار مثبت روی کاتد و یون های اکسیژن با بار منفی روی آند جمع میشوند. این روش از نظر اقتصادی جهت تولید گاز اکسیژن مقرون به صرفه نمی باشد.
فرایند الکترولیز آب نیاز به حرارت و جریان الکتریسیته دارد و لذا در چندین حالت دما بالا، فشار بالا و غیره انجام میشود. الکترولیز بخار که در دمای بالا انجام میشود، به منظور کاهش میزان الکتریسیته مصرفی مورد استفاده قرار میگیرد.
3- تولید اکسیژن به روش جذبی تحت فشار (PSA: Pressure Swing Adsorption )
در این روش هوا را تحت فشار جذبی توسط زئولیت خاص تفکیک می نمایند. به این صورت که هوا توسط یک کمپرسور تا ۶۰ PSI فشرده می شود. سپس این هوای فشرده وارد یک سیستم حاوی زئولیت شده تا طی فرایند مولکولار سیو (Sieve Molecular) یا همان غربال مولکولی قرار گیرد. نیتروژن وگازهای دیگر موجود در هوا تحت فشار، جذب حفره های مولکولی زئولیت شوند. آنچه جذب نمی شود گاز اکسیژن با خلوص ۹۹ تا ۹۹.۵% است. اکسیژن تولیدی با این روش مناسب برای مصارف پزشکی و فولاد سازی می باشد ولی خلوص لازم را برای برش کاری در حد عالی ندارد.
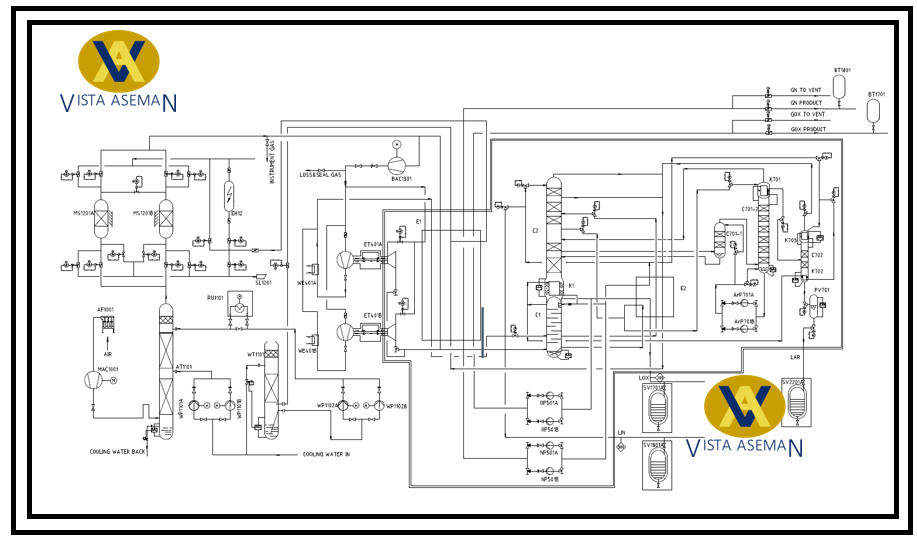
4- تولید اکسیژن به روش تقطیر جزء به جز توسط سپرتور هوا (ASU: Air Separation Unit)
در این روش هوا طی پنج مرحله به بشرح ذیل به مایع تبدیل و سپس عناصر تشکیل دهنده آن از هم جدا می شوند:
1- تراکم: Compression
2- تصفیه: Purification
3- خنک سازی: Refrigeration
4- انبساط: Expansion
5- تقطیر: Distillation
هوا توسط کمپرسورهای چند مرحله ای تا حدود ۲۰۰ بار فشرده میشود. پس از آن وارد سیستم تصفیه شده و ناخالصی های آن از جمله بخار آب، دی اکسید کربن و برخی هیدروکربن های همراه آن توسط زئولیت جذب و جدا میشوند. بعد هوای خشک و تصفیه شده توسط سیستم فریون جذب و جدا میشوند . هوای خشک و تصفیه شده توسط سیستم فریون تا منفی ۳۰ درجه سانتی گراد سرد می شود. پس از عبور از توربین اکسپندر و شیرهای انبساطی و همچنین افت فشار از ۲۰۰ به ۵ بار بسرعت سرد میشود . برودت آن به منفی ۱۷۰ درجه سانتی گراد میرسد. هوا با این دما که عمدتا به صورت مایع میباشد. وارد مرحله پنجم و ستون تقطیر می شود . در اینجا که قلب دستگاه تولید کرایوژنیک است عمل تقطیر و تفکیک جزء به جزء هوا شکل می گیرد. در حقیقت تقطیر یک فرایند تبخیر و انقباض دوباره است که برای جداسازی مخلوطی از مایعات از یکدیگر بر طبق نقطه جوششان استفاده می شود. لازم به یه یادآوری است که نقطه جوش اکسیژن در فشار اتمسفر ۱۸۴- درجه سانتیگراد، آرگون ۱۸۵- و نیتروژن ۹۶- درجه سانتیگراد می باشد. یعنی هر یک از عناصر یاد شده در این دماها از حالت گاز به مایع تبدیل میشوند. البته در برج تقطیر تحت فشار و حرارت بحرانی در دمای بالاتر از نقطه جوششان تبدیل به مایع می شود. اکسیژن یا نیتروژن بصورت گاز یا مایع که طبق این روش تولید می شود از نظر کمی و کیفی بهترین و مطمئن ترین روش است.
با مقایسه کلیه روشهای تولید در جدول ذیل به بررسی خروجی گاز های تولیدی در هر روش میپردازیم:
از جمع بندی روش های مختلف تولید گاز اکسیژن، نیتروژن و آرگون می توان دریافت که تولید همزمان هر سه گاز صرفاً از طریق تقطیر هوای مایع میسر است. این روش اصطلاحاً به کرایوژنیک موسوم است که شاخه ای از فیزیک است که در دماهای بسیار پایین کاربرد دارد. مزایای اقتصادی آن عبارتند از:
– قابلیت ذخیره سازی و حمل و نقل گاز به صورت مایع فشرده
– توانایی تولید ارزانتر و با خلوص بالای گازها
شرکت ویستا آسمان تامین کننده انواع کارخانه های تولید گاز اکسیژن،نیتروژن، آرگون و … از برترین برندهای اروپایی می باشد. جهت کسب اطلاعات بیشتر با واحد فروش شرکت ویستا آسمان تماس حاصل فرمایید.